Mis en ligne le 15 décembre 2016
Éditoriaux
Retour
La loi n° 2012-300 du 5 mars 2012 (dite loi Jardé) relative aux recherches impliquant la personne humaine a vu ses décrets d’application enfin promulgués le 16 novembre 2016 avec effet immédiat (Décret no 2016-1537). Dorénavant, toutes recherche sur la personne humaine en vue du développement des connaissances biologiques et médicales devront recevoir l’avis favorable d’un Comité de Protection des Personnes (CPP) tirés au sort après dépôt du dossier de recherche au près d’un « guichet unique » de la Direction Générale de la Santé (DGS). Pour obtenir la désignation aléatoire d’un CPP, les promoteurs de recherches cliniques doivent se connecter sur l’application VRB à l’adresse suivante : https://vrb.sante.gouv.fr.
Les Recherches sont maintenant classées en 3 catégories :
- Catégorie 1 : recherches interventionnelles (les recherches qui nécessite actuellement un avis d’un CPP). Dans cette catégorie, les recherches portant sur des médicaments relèveront dès 2018 du règlement européen (actuellement seuls les promoteurs volontaires peuvent tester en phase pilote cette réglementation). Les recherches de cette catégorie nécessitent une autorisation de l’ANSM (Agence national de sécurité du médicament) et un consentement écrit libre et éclairé par la personne se soumettant à la recherche.
- Catégorie 2 : recherches interventionnelles à risques et contraintes minimes. Ces recherches sont précisées par l’arrêté du 2 décembre 2016. On peut citer : attribution aléatoire de traitements ou d’actes dans leurs conditions habituelles d’utilisation(Etudes en soins courant dans l’ancienne législation), prélèvements sanguins veineux ou artériels dans des limites de volume par rapport au poids, prélèvements et collectes d’échantillons biologiques autre que du sang y compris des phanères et excréta, recueil de paramètres physiologiques par l’intermédiaire de capteurs, entretiens et questionnaires dont les résultats peuvent conduire à la modification de la prise en charge… Les recherches de cette catégorie nécessite un consentement exprès (écrit ou oral mais tracé) libre et éclairé et une simple information de l’ANSM.
- Catégorie 3 : recherches non interventionnelles, c’est à dire purement observationnelles (sans aucune intervention sur la prise en charge du patient). Ces études correspondent aux études hors loi Huriet dans l’ancienne législation, où un avis éthique pouvait être demandé à un IRB (comme le CERAR) en vue d’une publication. Ces recherches nécessitent une simple recherche de non opposition de la part du patient et une information de l’ANSM.
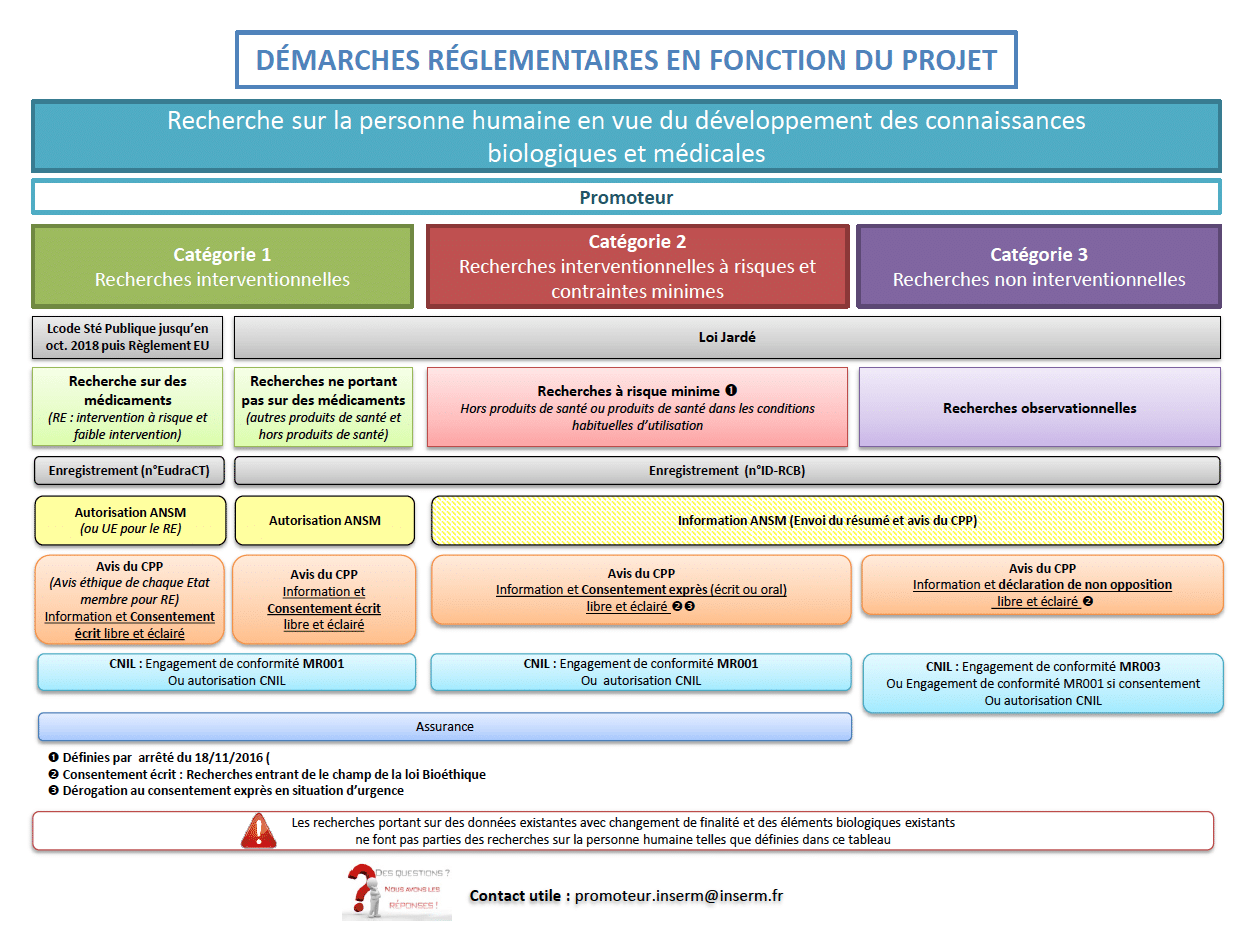 Source : Institut National de la santé et de la recherche médicale (Inserm)
Source : Institut National de la santé et de la recherche médicale (Inserm)
Consultez ce tableau récapitulatif sur le site de l’INSERM, en cliquant ici.
Les recherches considérées comme hors champs de la personne humaine sont les recherches sur registres, études statistiques ou données déjà existantes (dossiers standards). Il se pose alors la question du maintien d’un avis éthique en vue d’une publication ; la SFAR maintien donc le CERAR dans ces indications précises.
Il est clair que les « fausses » études rétrospectives (analyse à posteriori de l’introduction d’une intervention plus ou moins invasive non validée) ne peuvent faire partie de ces recherches. Ces études relevant d’un avis CNIL après avis du CCTIRS Comité Consultatif sur le Traitement de l’Information en matière de Recherche dans le domaine de la Santé) prochainement remplacé par le CEREES (Comité d’Expertise pour les Recherches, les Études et les Évaluations dans le domaine de la Santé). Ces avis sont d’ordre méthodologique sur la conservation des données, mais pas de nature éthique.
De nombreuses difficultés sont envisagées :
- La quantité de dossiers qui vont arrivés au « guichet unique » pourra t elle être gérée par le ministère?
- Comment les CPP, notamment ceux qui ne donnaient pas d’avis hors loi Huriet sur les études non interventionnelles vont ils traiter ces études ? un traitement plus « rapide » des avis sur les recherches de 2ieme et 3ième catégories est il envisageable ? La réponse des CPP devant intervenir dans les 40 jours qui suivent son dépôt.
- Faut il maintenir des avis éthiques « hors loi Jardé » pour les recherches rétrospectives pour satisfaire aux exigences des revues étrangères ?
Enfin, il faut préciser que toute demande d’avis sur des recherches ou des amendements avant la date du 17 novembre 2016 n’est pas concernée par cette nouvelle législation.
Nous pouvons juste espérer que cette nouvelle réglementation ne freine pas trop la recherche clinique française, l’avenir nous le dira.
Pr Jean-Etienne BAZIN


