Léger M et coll, Anesthesiology 2023 Nov 17. doi: 10.1097/ALN.0000000000004840.
Analyse par Christophe Aveline pour le Comité Scientifique de la SFAR
Contexte : Les bénéfices d’une stratégie excluant les opiacés en peropératoire (OFA) demeurent insuffisamment définis. Deux méta-analyses récentes ont identifié un risque supérieur d’effets secondaires associés aux opiacés par rapport à l’OFA (1, 2). Dans l’étude POFA, prématurément interrompue après observation d’effets secondaires attribués à la dexmédétomidine administrée sans protocole strict, le risque relatif (RR) mesuré sur le critère principal (hypoxie + iléus + troubles cognitifs) était en défaveur de l’OFA (RR 1,16 [IC95% 1,01-1,33]) (3).
L’étude SOFA a testé l’hypothèse d’une supériorité de l’OFA sur la qualité de récupération postopératoire par rapport à un groupe contrôle (C) recevant des opiacés en peropératoire.
Méthodes :
Étude randomisée contrôlée, adultes opérés d’une chirurgie non cardiovasculaire et non ostéoarticulaire supérieure à 90min. Randomisation (07/2021-2/2022) par algorithme prenant en compte le type et la sévérité des interventions. Patients et évaluateurs en postopératoire non informés de la randomisation.
- Groupe OFA : clonidine 50µg/h avant induction puis 100-150µg/h (arrêt en fin d’intervention), après induction magnésium 40mg/kg + kétamine 0,5mg/kg puis 0,2mg/kg/h (stoppé 30min avant fermeture) + lidocaïne 1,5mg/kg puis 1,5mg/kg/h (stoppée 1h après extubation).
- Groupe C : à l’appréciation du praticien, sufentanil 0,1-0,3µg/kg ou rémifentanil 3-6ng/ml + bolus unique de kétamine 0,15mg/kg ± oxycodone/morphine 1-5mg.
- Dans les deux groupes : en peropératoire, paracétamol 1g ± kétoprofène 100mg ± néfopam 20mg. Induction et entretien de l’anesthésie, prévention antiémétique à l’appréciation des médecins sans protocolisation, titration en SSPI (oxycodone).
Critère de jugement principal (CJP) : score multidimensionnel QoR-15 à H24
Critères secondaires : score QoR-15 à H48 et H72, douleur à la mobilisation, complications (classification POMS), consommation analgésique postopératoire, variations de pression artérielle (PA) et fréquence cardiaque (FC) peropératoire, nausées/vomissements, durée de séjour et score de satisfaction patients/chirurgiens. A M3 : score de qualité de vie EQ-5D-3L, incidence de douleur chronique (Brief Pain Inventory) et douleur neuropathique (DN4).
Compliance à la randomisation :
Groupe OFA : au moins 2/4 des analgésiques du protocole quelques soit la dose ni interruption de l’administration et absence d’opiacé peropératoire.
Groupe C : absence de lidocaïne, clonidine ou magnésium.
Calcul d’effectif et statistiques :
Amélioration de 8 points du score QoR-15 à H24 dans le groupe traitement (risque α=0,05, puissance 80%) à partir d’une valeur de QoR-15 de 97±16 à H24 (4), 63 patients/groupe requis (test bilatéral).
Analyse en intention de traiter (ITT) et en per-protocole (PP) selon la compliance, régression séquentielle et imputation multiple des valeurs manquantes sur le CJP, les scores EQ-5D-3L et BPI. Analyse séquentielle hiérarchique pour réduire le risque d’inflation du risque α sur l’analyse des scores QoR-15 après H24. Analyse par régression linéaire par effet fixe et aléatoire pour tenir compte de l’influence de l’interaction temps-cofacteurs sur les scores de douleur et la consommation d’opiacé. Analyse des critères qualitatifs par régression logistique.
Résultats : 136 patients (OFA : 65, C : 68) analysés en ITT, sexe féminin 87%, chirurgie plastique 64%, ASA1 53%, halogéné 96%, prévention NVPO 93%. Les compliances respectives dans les groupes OFA et C de 87% et de 83%, différences démographiques mineures (support BIS dans le groupe OFA 31% vs 9% ; infiltration peropératoire groupe OFA 37% vs 54%).
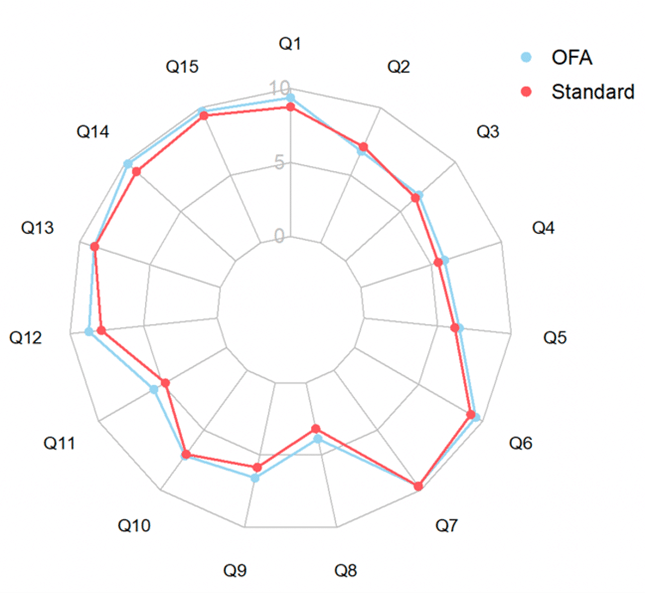
CJP : amélioration du score QoR-15 dans le groupe OFA (différence moyenne 6,2 [IC95% 0,4-12] – Fig. 1) sans différence en PP (5,1 [IC95% -1/11,3]).
Critères secondaires :
- Amélioration QoR-15 à H48 (ITT : 8,7 [IC95% 2,9-14,5]) et à H72 (ITT : 7,3 [IC95% 1,6-13]).
- Analyse en sous-groupe QoR-15 à H24 en faveur de l’OFA pour la chirurgie complexe et les sujets > 60 ans, à H48 chez les femmes et en chirurgie majeure, à H72 chez les femmes, en chirurgie majeure, ORL et gynécologique.
- Absence de différences sur la consommation d’opiacé, scores de douleur H0-H72, satisfaction praticiens/patients, douleur à M3 (OFA : différence -9,8% [IC95% -25,2%/5,6%], douleur neuropathique (OFA : 8% ; C : 18,5%) et qualité de vie.
- Différences de risques non significatives : hypotension artérielle <90mmHg plus de 5min, bradycardie <50b/min, recours aux catécholamines, respectivement 1,7% [IC95% -14,8%/18,2%] ; -2,9% [-7%/1,1%] ; 9,7% [-2,4%/21,8%].
- Incidence plus élevée de PAS > 160mmHg sur plus de 5min dans le groupe OFA (13,8% vs 2,9% en ITT ; 16,4% vs 1,8% en PP) et FC > 140b/min (4,6% vs 0 en ITT, ns en PP).
- Proportion de patients sans complications (POMS=0) à H24 supérieure dans le groupe OFA (37% vs 19%). Réduction des effets secondaires imputables au protocole dans le groupe OFA (12,3% vs 27,9%), du séjour en SSPI (2,2h [1,6-2,5] vs 1,8h [1,4-2,1]) et du délai de reprise du transit (5j [4-6] vs 5j [5-7]) sans impact sur la durée de séjour.
Discussion : Dans cette étude, l’OFA améliore la qualité de récupération entre H0 et H72 après chirurgie générale sans, cependant, influencer la douleur à la mobilisation, la consommation d’opiacé, les NVPO et la durée d’hospitalisation. Ces résultats confirment les bénéfices de l’OFA observés sur les scores QoR-15 et QoR-40 en chirurgie générale (1, 2, 6, 7). Malgré une amélioration du CJP, la douleur à la mobilisation est similaire dans les deux groupes, l’utilisation d’anesthésies locorégionales, non autorisée dans l’étude POFA (3), ayant probablement influencée la période postopératoire immédiate. Contrairement à la dexmédétomidine (3), la clonidine n’a pas été associée à un surcroit d’hypotension artérielle ou de bradycardie peropératoire, ni d’excès de sédation et d’évènements hypoxiques postopératoire (OFA vs C : -23,9% [IC95% -7/1,1]. On retrouve même une réduction des effets indésirables dans le groupe OFA (-15,6% [IC95% -29%/-2,3%]) et l’analyse exploratoire identifie une proportion plus importante de patients sans complications (POMS=0) à H24. Bien que significatif, l’ampleur d’effet sur le CJP est inférieure à celle définie pour le calcul d’effectif ainsi qu’à la valeur minimale de 8 points jugée relevante (5). Néanmoins, l’effet sur le CJP en ITT persiste après H24 et le plan statistique a utilisé une méthodologie robuste prenant en compte le risque d’influence de facteurs confondants.
Cet essai a inclus des patients à faible comorbidité (95% d’ASA 1-2), majoritairement de sexe féminin et opérés de chirurgie gynécologiques/plastiques pour près de 80% d’entre eux. L’absence de différences sur l’incidence des douleurs chroniques et neuropathiques à M3 est probablement en lien avec le profil des patients et des interventions réalisées ainsi qu’à l’absence de dimensionnement à priori pour ces objectifs. La compliance de la randomisation inférieure à 90% reflète la variabilité d’adhésion des praticiens à l’OFA dans une étude au design pragmatique. L’absence d’aveugle du médecin en charge de l’anesthésie et la possibilité de modifier le protocole alloué par la randomisation chez des patients qu’il jugeait non éligibles (15% d’opiacé dans le groupe OFA, 15% de lidocaïne dans le groupe C) a pu influencer la non-concordance des résultats entre ITT et PP. Enfin, le caractère monocentrique introduit une variabilité inter-individuelle inhérente à la réalisation de l’OFA dans une étude pragmatique.
Implications : L’OFA associant analgésie systémique et locorégionale chez des patients présentant une trajectoire douloureuse modérée après chirurgie générale constitue une stratégie adéquate qui ne doit, cependant, pas faire éliminer définitivement les opiacés de nos pratiques (8). Le choix d’une stratégie périopératoire doit permettre la détection dès la phase préopératoire des patients à risque de douleur élevée ou de difficulté de réhabilitation, éléments non abordés dans cette étude.
- Lancet 2022; 399 (10343): 2280-2293
- Acta Anaesthesiol Scand 2022; 66: 170-185.
- 2021 ; 134: 541-551.
- Br J Anaesth. 2020; 125: e345‑7
- Anesthesiology 2016; 125: 39-45.
- Drug Des Devel Ther.2023; 17: 3539–3547
- Eur J Anaesthesiol 2023; 40: 552-9.
- JAMA Surg 2023; 158: 854-64.
Fig. 1 : Radar plot des paramètres (bien-être physique et mental, 15 questions, scores 0-150) constituant le score QoR-15 à H24.